Our website is made possible by displaying online advertisements to our visitors.
Please consider supporting us by disabling your ad blocker.
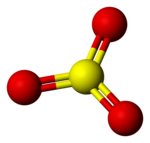
Anidride solforica
| Anidride solforica | |
|---|---|
 | |
 | |
| Nome IUPAC | |
| triossido di zolfo | |
| Nomi alternativi | |
| anidride solforica | |
| Caratteristiche generali | |
| Formula bruta o molecolare | SO3 |
| Massa molecolare (u) | 80,06 |
| Aspetto | solido cristallino incolore (forma α) |
| Numero CAS | |
| Numero EINECS | 231-197-3 |
| PubChem | 24682 |
| SMILES | O=S(=O)=O |
| Proprietà chimico-fisiche | |
| Densità (g/cm3, in c.s.) | 1,97 (forma γ) |
| Solubilità in acqua | reagisce |
| Temperatura di fusione | 62,2 °C (335,35 K) (forma α) |
| Temperatura di ebollizione | decompone a 50 °C (323,15 K) (forma α) |
| Tensione di vapore (Pa) a 293,15 K | 37333 (forma γ) |
| Proprietà termochimiche | |
| ΔfH0 (kJ·mol−1) | −397,77 |
| S0m(J·K−1mol−1) | 256,77 |
| C0p,m(J·K−1mol−1) | 24,02 |
| Indicazioni di sicurezza | |
| Simboli di rischio chimico | |
   
| |
| pericolo | |
| Frasi H | 271 - 314 - 330 - 350 |
| Consigli P | 201 - 220 - 260 - 280 - 284 - 305+351+338 [1] |
Il triossido di zolfo o anidride solforica è un composto chimico corrosivo che reagendo con acqua produce acido solforico, essendo la sua anidride. Esiste in tre forme: le forme α e β sono dei solidi in condizioni normale, mentre la forma γ è un liquido. Il triossido di zolfo gassoso presente nell'atmosfera rappresenta la causa primaria delle piogge acide.
Dal punto di vista strutturale si tratta di una molecola trigonale planare (stato gassoso) ipervalente. Il doppio legame S=O misura 142 pm.
- ^ Sigma Aldrich; rev. del 13.01.2012
Previous Page Next Page


