Our website is made possible by displaying online advertisements to our visitors.
Please consider supporting us by disabling your ad blocker.
Nitrogena dioksido
| Nitrogena duoksido | |||||
 | |||||
| Plata kemia strukturo de la Nitrogena dioksido | |||||
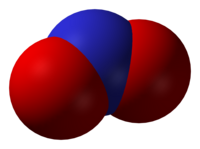 | |||||
| Tridimensia kemia strukturo de la Nitrogena dioksido | |||||
| Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | |||||
| CAS-numero-kodo | 10102-44-0 | ||||
| ChemSpider kodo | 2297499 | ||||
| PubChem-kodo | 3032552 | ||||
| Merck Index | 15,6690 | ||||
| Fizikaj proprecoj | |||||
| Aspekto | toksa, irita, venena, koroda, oksidiga, alte reakciema, ruĝbruna gaso kun penetranta klorsimila odoro | ||||
| Molmaso | 46,005 g·mol-1 | ||||
| Denseco | 3,3g cm−3 | ||||
| Fandpunkto | -11,2°C | ||||
| Bolpunkto | 21,1°C | ||||
| Refrakta indico | 1,449 | ||||
| Solvebleco | Akvo:reakcias | ||||
| Sekurecaj Indikoj | |||||
| Riskoj | R26 R34 | ||||
| Sekureco | S9 S26 S28 S36/37/39 S45 | ||||
| Pridanĝeraj indikoj | |||||
| Danĝero
| |||||
| GHS Damaĝo Piktogramo |
| ||||
| GHS Signalvorto | Damaĝa substanco | ||||
| GHS Deklaroj pri damaĝoj | H270, H280, H319, H330, H336, H361, H370, H372 | ||||
| GHS Deklaroj pri antaŭgardoj | P201, P202, P220, P244, P260, P261, P264, P270, P271, P280, P281, P284, P304+340, P305+351+338, P308+313, P310, P314, P320, P321, P337+313, P370+376, P403, P403+233, P405, P410+403, P501[2] | ||||
(25 °C kaj 100 kPa) | |||||
Nitrogena dioksido, aŭ foje nitrogena duoksido, (molekula formulo NO2) estas neorganika nitrogena kombinaĵo de oksigeno, toksa, venena, ruĝbruna gaso kun klorsimila odoro, kiu reakcias kun la atmosfero por formi nitratan acidon, kontribuante por generado de la acida pluvo. Ĝi estas respondeca pri kaŭzado de fluidaĵo-akumuliĝo en la pulmoj. Krom tio, nitrogena dioksido plenumas rolon en la formado de fotokemia fumnebulo, ia duonruĝe bruna atmosfera kondiĉo tre ofte vidata en urbareoj kaj kreita de agado de la sunlumo al sur la malalta atmosfero.
- ↑ https://www.reta-vortaro.de/revo/ Vd nitrogeno-n en ReVo, ĉar la fundamenta vorto "azoto" prefereblas.
- ↑ PubChem
Previous Page Next Page










